About
The Bacterial infections: antimicrobial therapies group is a senior group.
Infectious diseases constitute a tenacious and major public health problem all over the world. The emergence and increasing prevalence of bacterial strains that are resistant to available antibiotics demand the discovery of new therapeutic approaches.
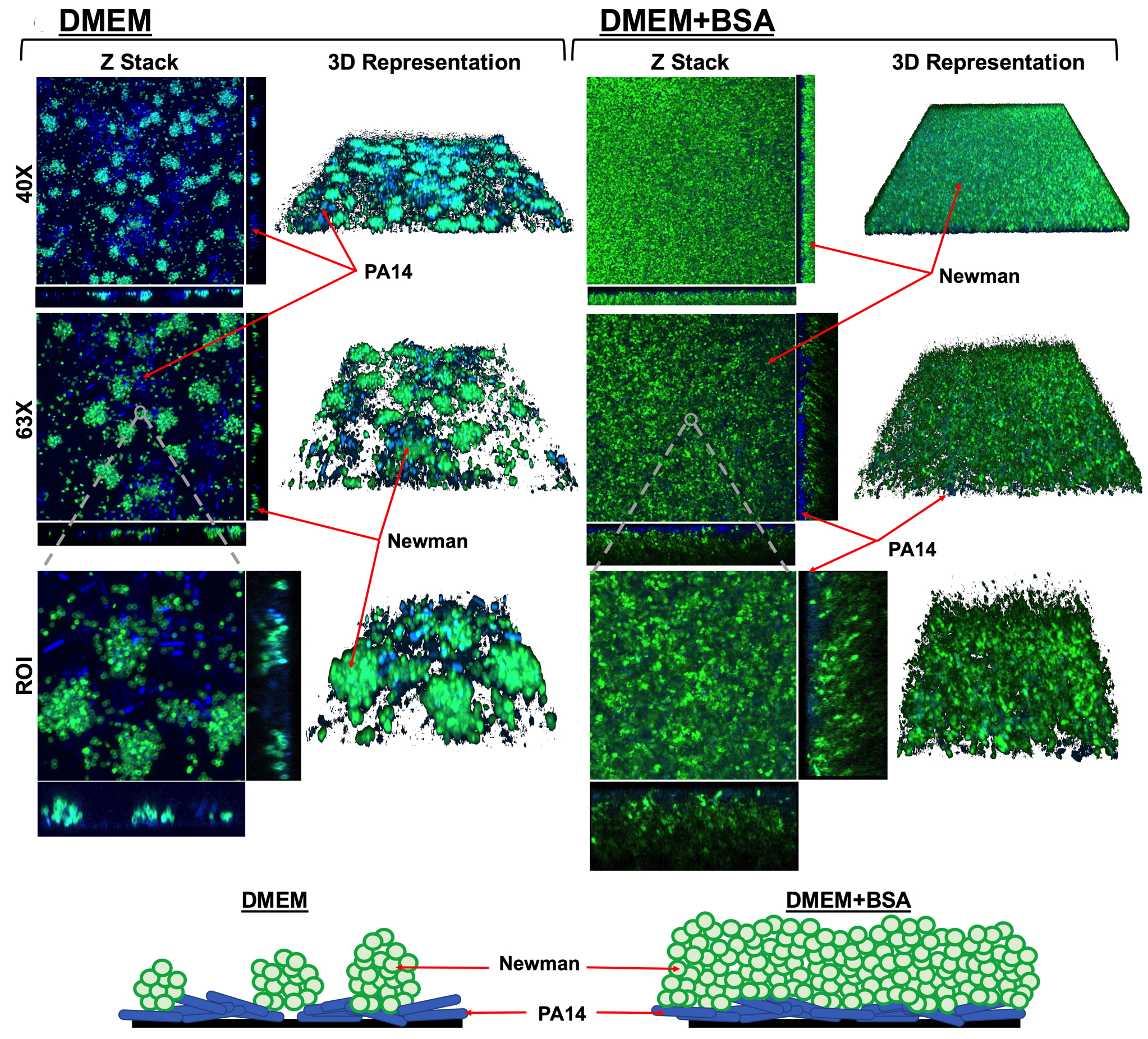
Biofilms are bacterial communities that grow embedded within a protective matrix produced by themselves.
Chronic infections caused by bacteria growing in biofilms, are enormously complicated to treat. It increases their fitness and survival, thus complicating treatment and diagnosis because they persist despite the action of antibiotic therapies and adaptive immune responses.
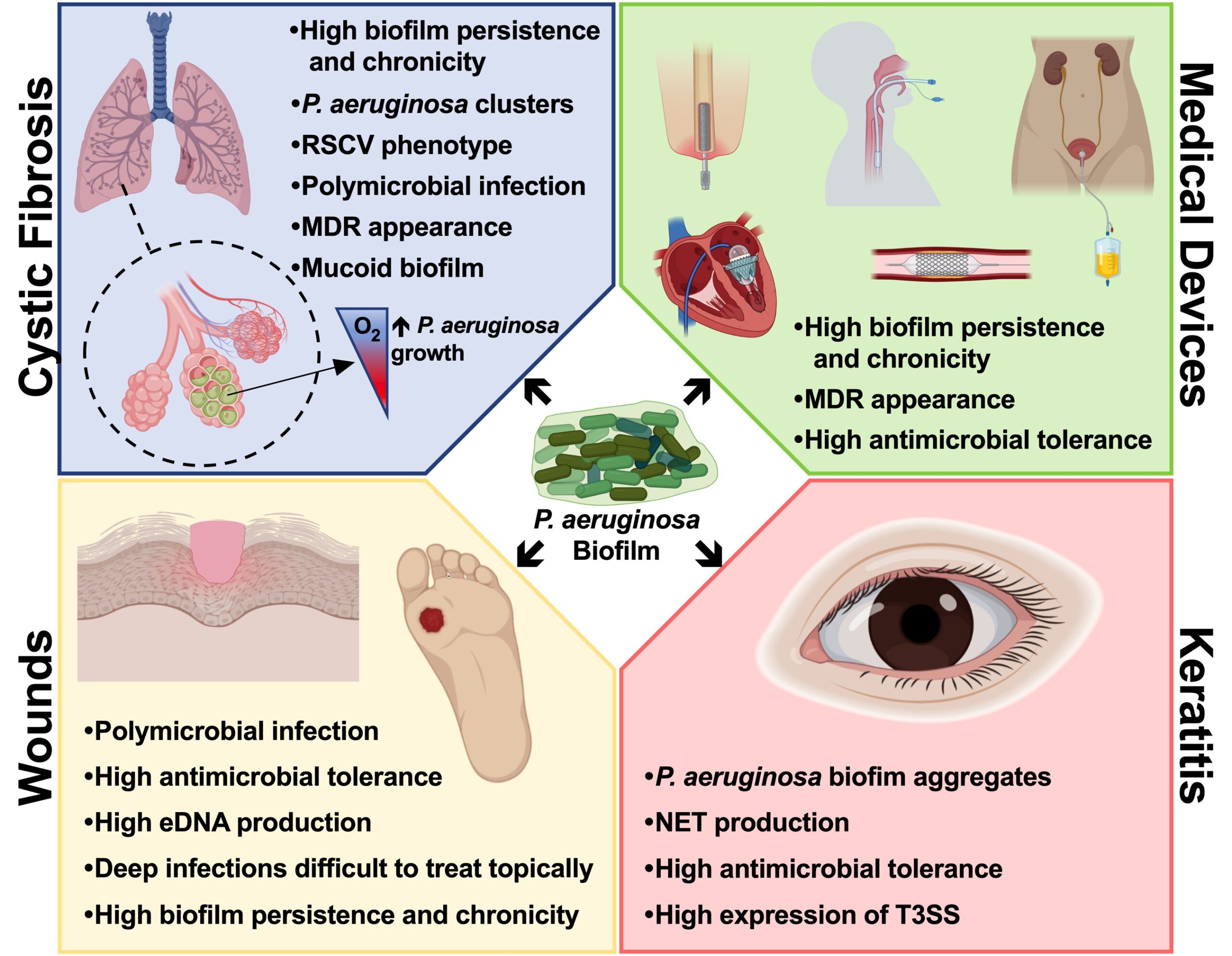
Over 60% of all human infections are characterized by the formation of a biofilm, which is involved in a wide variety of pathological conditions by either growing over human tissues (Cystic Fibrosis, Chronic Obstructive Pulmonary Disease, chronic wound, etc.) or by developing on the surfaces of medical devices (e.g. endotracheal tubes, intravenous and urinary catheters, etc.).
Our lab aims to investigate new antimicrobial therapies and strategies to combat bacterial infections with different objectives:
- The use of nanomedicine techniques for the development of novel and specific nanoparticles to deliver existing antibiotics or new identify antimicrobial drugs, significantly when the bacteria are growing in biofilm, close to the physiological conditions of the disease and where the current chemotherapy fails;
- The identification and screening of new molecules for the highly selective inhibition of new antibacterial targets (e.g. ribonucleotide reductases);
- The use of nanomedicine techniques for the development of novel and specific nanoparticles to deliver existing antibiotics or new identify antimicrobial drugs, significantly when the bacteria are growing in biofilm, close to the physiological conditions of the disease and where the current chemotherapy fails;
- To study new methodologies to treat chronic bacterial infections in patients suffering cystic fibrosis;
- To develop a new family of antibacterial vaccines;
- The development of new strategies for bacterial coculture systems;
- To study and develop models for wound healing infections and the search of novel treatments;
- The use of lab-on-a-chip technology to deeply elucidate mechanisms to combat bacterial forming biofilm as well as new approaches to identify multiresistant bacteria to different antibiotics.
- To establish the molecular basis for the regulation of genes involved in DNA synthesis (ribonucleotide reductase genes), their importance in virulence and biofilm formation;
We believe these projects will be beneficial to society since we explore the use of different bioengineering approaches to elucidate ways to diagnose and eradicate multi-drug resistant bacteria.
Related links:
Staff
Former Members
Maria del Mar Cendra | PhD Student
Projects
| NATIONAL PROJECTS | FINANCER | PI |
|---|---|---|
| InfectTreat · Understanding DNA metabolism and new insights in polymicrobial biofilms: development of more efficient therapies to tackle bacterial infections (2022 – 2025) | MICIU. Generación Conocimiento proyectos I+D | Eduard Torrents |
| DISnanoAMR · Desarrollo de nuevas estrategias para hacer frente a la resistencia antibiótica (2022 – 2025) | MICIU. Poryectos de I+D+i en líneas estratégicas | Eduard Torrents |
| IVD-Biofilm · Desarrollo de un nuevo dispositivo para el diagnóstico personalizado en infecciones relacionadas con biopelículas (2022 – 2024) | MICIU. Proyectos Pruebas de Concepto | Eduard Torrents |
| Acuerdo de colaboración ente el IBEC y la Asociación Catalana de Fibrosis Quística (2019 – 2024) | Asociación Catalana de Fibrosis Quística | Eduard Torrents |
| Las biopelículas polimicrobianas para el desarrollo de terapias más eficientes contra las infecciones bacterianas” (2021-2022) | Diputació de Barcelona | Eduard Torrents |
| combatRNR · Comprender la síntesis del ADN en patógenos bacterianos: nuevas estrategias para el tratamiento de enfermedades infecciosas (2019 – 2022) | MICIU. Retos investigación: Proyectos I+D | Eduard Torrents |
| BIOVAC · Artificial bacteria: a novel generation of bioinspired vaccines (2020 – 2023) | BIST. BIST Ignite Program | Eduard Torrents |
| Las biopelículas polimicrobianas para el desarrollo de terapias más eficientes contra las infecciones bacterianas” (2021-2022) | Diputació de Barcelona | Eduard Torrents |
| FINISHED PROJECTS | FINANCER | PI |
|---|---|---|
| Terapias alternativas para el tratamiento de las infecciones bacterianas crónicas en pacientes con fibrosis quística a (2019-2021) | Asociación Catalana de Fibrosis Quística | Eduard Torrents |
| Noves estratègies antimicrobianes per combatre la fibrosi quística (2016-2020) | Obra Social La Caixa | Eduard Torrents |
| BiofilmChip CaixaImpulse BiofilmChip (2018 – 2020) | Obra Social La Caixa | Eduard Torrents |
| Desarrollo de una nueva familia de compuestos antimicrobianos | Asociación Catalana de Fibrosis Quística | Eduard Torrents |
| Identificación y administración de nuevas moléculas antimicrobianas contra Pseudomonas aeruginosa creciendo en biofilm | Asociación Española Fibrosis Quística, Becas de Investigación “Pablo Motos” | Eduard Torrents |
| Novel strategies to combat bacterial chronic infections by the development of microfluidics platforms to analyse and treat bacterial growing in biofilms (2016) | Obra Social La Caixa | Eduard Torrents |
| Redes reguladoras de la expresión génica de las distintas ribonucleotidil reductasas en bacterias | MINECO, I+D-Investigación fundamental no orientada | Eduard Torrents |
| BACTSHOT Novel antimicrobial therapy (2016-2017) | EIT Health Head Start – Proof of Concept | Eduard Torrents |
| inhibitRNR Las ribonucleotido reductasas como una nueva diana terapéutica frente a patógenos bacterianos (2016-2018) | MINECO, Retos investigación: Proyectos I+D | Eduard Torrents |
| Ribonucleotide reductasas: una nueva diana terapéutica contra organismos patógenos en enfermos de fibrosis quística (2010-2017) | Asociación Española Fibrosis Quística, Becas de Investigación “Pablo Motos” | Eduard Torrents |
| RNRbiotic New strategy to combat bacterial infections (2015-2017) | Obra Social La Caixa, Caixaimpulse | Eduard Torrents |
Publications
(See full publication list in ORCID)
[br]
Equipment
- Zeiss LSM 800 Confocal Laser Scanning Microscope
- Nikon Inverted Fluorescent microscope ECLIPSE Ti-S/L100
- Cell culture facilities for microbial infections
- Characterization of nanoparticles/biomaterial antibacterial activity
- Drosophila melanogaster and Galleria mellonella as a model host for bacterial infections
- Continuous flow system model for bacterial biofilm development
- Single Channel Fiber-Optic Oxygen Meter with microsensor
- Molecular biology, biochemistry and protein purification facilities
- Bacterial expression systems for heterologous protein production
Collaborations
- Prof. Daniel Ruiz
Català de Nanociència i Nanotecnologia (ICN2), Barcelona, Spain - Prof. Bianca Sclavi
NRS Biologie Computationnelle et Quantitative. Sobornne Université. Paris. France - Dr. Esther Julián
Dept. de Genètica i de Microbiologia, Universitat Autònoma de Barcelona, Spain - Prof. Josep Samitier
IBEC - Prof. Santiago Vazquez
Laboratori de química farmacèutica, Pharmacy Faculty, Barcelona University - Prof. Gabriel Gomila
IBEC - Dr. Maarten Fauvart
IMEC, Leuven, Belgium
News

Un pas endavant en l’ús de nanopartícules per combatre la resistència bacteriana
El grup d’Infeccions Bacterianes: Teràpies Antimicrobianes, liderat per Eduard Torrents, ha dissenyat un nou mètode que permet, per primera vegada, comprovar l’eficàcia dels fàrmacs antimicrobians que inclouen nanopartícules en la seva estructura. Aquesta nova tècnica, s’ha publicat recentment en la revista Journal of Nanobiotechnology. La resistència bacteriana és una de les majors amenaces a què s’enfronta la salut global en l’actualitat. Segons dades de l’OMS, cada vegada hi ha més infeccions (pneumònia, tuberculosi, gonorrea) el tractament de les quals s’ha complicat a causa de la pèrdua d’eficàcia de molts antibiòtics. L’origen d’aquest problema es troba en l’ús indegut i abusiu dels antibiòtics, que provoca que els bacteris es tornin resistents a ells.
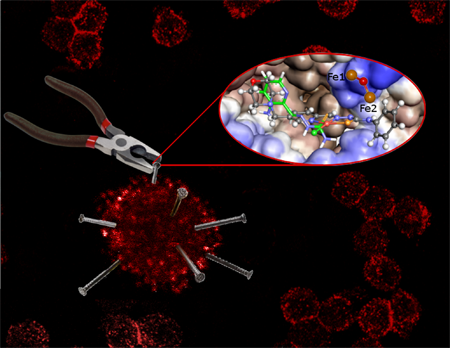
Dues vies prometedores en la lluita contra la resistència als antibiòtics
El grup Infeccions bacterianes: teràpies antimicrobianes de l’IBEC ha publicat dos articles en què ofereix noves esperances per a la recerca urgent d’antimicrobians. “Necessitem antimicrobians desesperadament”, afirma l’investigador principal del grup, Eduard Torrents. “La resistència als antibiòtics és una de les amenaces actuals més importants per a la salut humana, i ja s’acosta el moment en què tota una sèrie de procediments rutinaris poden tornar-se molt més arriscats”. No només algunes infeccions o malalties comunes s’han tornar resistents als antibiòtics que habitualment s’usaven per tractar-les, sinó que ara s’hi afegeix un problema mèdic altament urgent: el ràpid augment dels anomenats “superbacteris” o bacteris multi resistents, que són immunes a pràcticament tots els antibiòtics que tenim actualment al nostre abast.

“Ajudes de la Fundació Bancària “La Caixa” a 75 projectes d’investigació”
IBEC group leader Eduard Torrents appeared on TV3’s Telenotícies on Monday night explaining his BiofilmChip project that has been funded with a CaixaImpulse grant.

Cinc investigadors de l’IBEC guardonats en la cerimònia de les beques “la Caixa”
Cinc investigadors de l’IBEC van rebre ahir les beques de “la Caixa” a les convocatòries de recerca i innovació. Anna Labernadie i Irene Marco, estudiants postdoctorals dels grups de l’IBEC Integrative Cell and Tissue Dynamics i Biosensors for Bioengineering, respectivament, han obtingut les beques de la primera convocatòria del programa Junior Leader de “la Caixa”, que ajuda investigadors i investigadores destacats, de qualsevol nacionalitat, que vulguin continuar la seva carrera de recerca en territori espanyol o portuguès. L’Anna ha estat una de les 10 estudiants postdoctorals en aconseguir una beca de la modalitat “Retaining” per a candidats que ja resideixen a Espanya, i la Irene ha estat guardonada amb una de les 20 beques de la modalitat “Incoming” per a candidats residents a l’estranger.
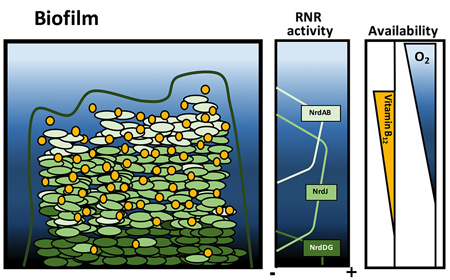
Els bacteris també necessiten vitamines
El grup de l’IBEC Bacterial infections: antimicrobial therapies ha revelat el paper essencial que exerceix una vitamina en el desenvolupament de biopel·lícules bacterianes. Aquest nou descobriment podria ajudar a comprendre com es propaguen aquests bacteris, la qual cosa ajudarà a dissenyar millors fàrmacs antibacterians específics. L’espècie bacteriana P. aeruginosa causa infeccions pulmonars cròniques en pacients amb fibrosis quística o malaltia pulmonar obstructiva crònica (MPOC) en formar una biopel·lícula madura, on les cèl·lules s’adhereixen entre si i poden ocupar moltes superfícies diferents, la qual cosa els permet créixer i adaptar-se.


 ibecbarcelona.eu
ibecbarcelona.eu