Un equip internacional codirigit per l’Institut de Bioenginyeria de Catalunya (IBEC) i l’Hospital West China de la Universitat de Sichuan (WCHSU) va poder revertir l’Alzheimer en ratolins després de només 3 injeccions amb nanopartícules. L’enfocament innovador per tractar la malaltia se centra a restaurar la funció normal del sistema vascular, en lloc d’actuar sobre les neurones o altres cèl·lules cerebrals, com s’ha fet habitualment fins ara. Aquest assoliment, publicat a la revista Signal Transduction and Targeted Therapy, és un pas prometedor cap a un tractament eficaç per a la malaltia d’Alzheimer.

Un equip de recerca codirigit per l’Institut de Bioenginyeria de Catalunya (IBEC) i l’Hospital West China de la Universitat de Sichuan (WCHSU) en col·laboració amb investigadors del Regne Unit, ha demostrat una estratègia basada en nanotecnologia que reverteix la malaltia d’Alzheimer en ratolins. A diferència de la nanomedicina tradicional, que es basa en nanopartícules com a portadores de molècules terapèutiques, aquest enfocament utilitza nanopartícules que són bioactives per si soles: “fàrmacs supramoleculars”. En lloc de dirigir-se directament a les neurones, la teràpia restaura la funció adequada de la barrera hematoencefàlica (BBB per les seves sigles en anglès), el “guardià vascular” que regula l’entorn del cervell. En reparar aquesta interfície crítica, els investigadors van aconseguir revertir la patologia de l’Alzheimer en models animals.
Només 1 hora després de la injecció observem una reducció del 50-60% en la quantitat d’Aβ dins del cervell.
Junyang Chen
El cervell és l’òrgan més car del cos, consumint el 20% de l’energia en adults i fins al 60% en nens. Aquesta energia arriba a través d’un vast subministrament de sang, assegurat per un sistema vascular únic i dens on cada neurona es nodreix d’un capil·lar. El nostre cervell conté aproximadament mil milions de capil·lars, cosa que destaca el paper vital del sistema vascular cerebral en el manteniment de la salut i la lluita contra les malalties. Aquestes troballes ressalten el paper crucial de la salut vascular, especialment en malalties com la demència i l’Alzheimer, que es relacionen amb un sistema vascular compromès.
La BBB és una barrera cel·lular i fisiològica que separa el cervell del flux sanguini per protegir-lo de perills externs com patògens o toxines. L’equip d’investigadors va demostrar que enfocar a un mecanisme específic permet que les “proteïnes de rebuig” indesitjades produïdes al cervell travessin aquesta barrera i s’eliminin en el flux sanguini correctament. En la malaltia d’Alzheimer, la principal proteïna “de rebuig” és l’amiloide-β (Aβ), l’acumulació de la qual perjudica el funcionament normal de les neurones.
Els investigadors van utilitzar models de ratolí que estan programats genèticament per produir majors quantitats de proteïna Aβ i desenvolupar un deteriorament cognitiu significatiu que imita la patologia de l’Alzheimer. Van administrar només 3 dosis dels fàrmacs supramoleculars i posteriorment van monitorar regularment l’evolució de la malaltia. “Només 1 hora després de la injecció observem una reducció del 50-60% en la quantitat d’Aβ dins del cervell“, explica Junyang Chen, primer coautor de l’estudi, investigador de l’Hospital West China de la Universitat de Sichuan i estudiant de doctorat del University College London (UCL).
L’efecte a llarg termini prové de la restauració del sistema vascular del cervell. El més rellevant és que les nostres nanopartícules actuen com un fàrmac i semblen activar un mecanisme de retroalimentació que retorna aquesta via d’eliminació a nivells normals.
Giuseppe Battaglia
Les dades més destacades van ser els efectes terapèutics. Els investigadors van realitzar diversos experiments per analitzar el comportament dels animals i mesurar el deteriorament de la memòria durant diversos mesos, cobrint totes les etapes de la malaltia. En un dels experiments, van tractar un ratolí de 12 mesos (equivalent a un humà de 60 anys) amb les nanopartícules i van analitzar el seu comportament després de 6 mesos. El resultat va ser impressionant: l’animal, de 18 mesos (comparable a un humà de 90 anys), havia recuperat el comportament d’un ratolí sa.
“L’efecte a llarg termini prové de la restauració del sistema vascular del cervell. Creiem que funciona com una cascada: quan s’acumulen espècies tòxiques com la beta amiloide (Aβ), la malaltia progressa. Però una vegada que la vascularització pot funcionar novament, comença a eliminar Aβ i altres molècules perjudicioses, cosa que permet que tot el sistema recuperi el seu equilibri. El més rellevant és que les nostres nanopartícules actuen com un fàrmac i semblen activar un mecanisme de retroalimentació que retorna aquesta via d’eliminació a nivells normals.“
Giuseppe Battaglia, professor de recerca ICREA a l’IBEC, investigador principal del Grup de Biònica Molecular i líder de l’estudi.
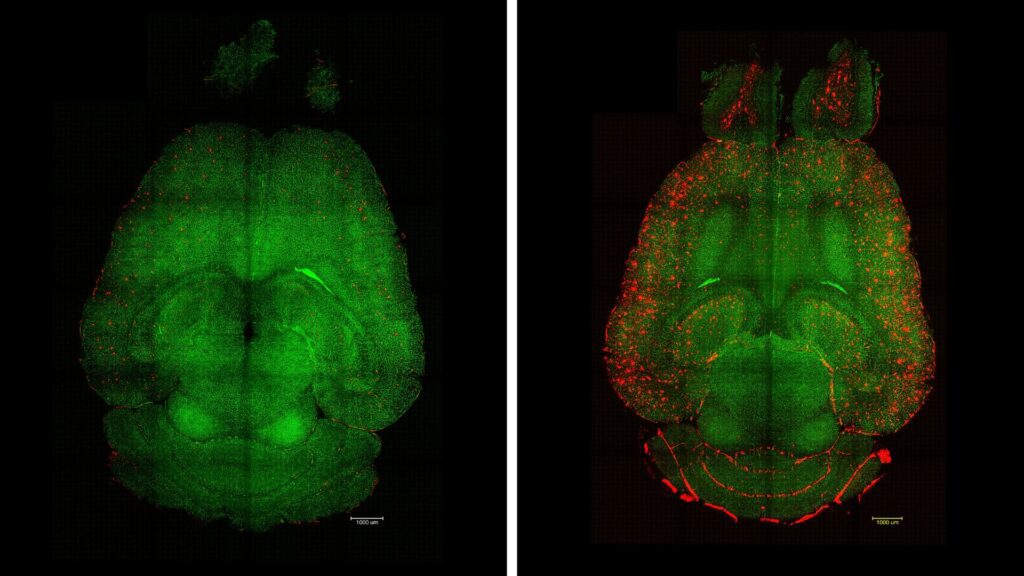
Eliminació d’amiloide-β del cervell
En la malaltia d’Alzheimer, un dels problemes clau és que el sistema natural d’eliminació del cervell per a toxines com la proteïna amiloide-β deixa de funcionar correctament. Normalment, la proteïna LRP1 actua com un guardià molecular: reconeix Aβ, s’hi uneix per lligands i la transporta a través de la barrera hematoencefàlica cap al torrent sanguini, on es pot eliminar. Però aquest sistema és fràgil. Si LRP1 s’uneix a massa Aβ i amb massa força, el transport s’obstrueix i la proteïna mateixa es degrada dins de les cèl·lules de barrera hematoencefàlica, deixant menys LRP1 “portadors” disponibles. En contra, si s’uneix a molt poca Aβ, el senyal és massa feble per activar el transport. En tots dos casos, el resultat és el mateix: Aβ s’acumula dins del cervell.
Els fàrmacs supramoleculars desenvolupats en aquest treball actuen com un interruptor que restableix el sistema. En imitar els lligands de LRP1, poden unir-se a Aβ, creuar la barrera hematoencefàlica i iniciar el procés d’eliminació d’espècies tòxiques del cervell. D’aquesta manera ajuden a restaurar el paper natural del sistema vascular com a via de neteja de residus i restableixen la seva funció adequada.

Nanopartícules per tractar l’Alzheimer
En aquest estudi, els investigadors introdueixen nanopartícules que actuen com a fàrmacs supramoleculars, agents terapèutics per si sols en lloc de portadors de medicaments. Dissenyades amb un enfocament d’enginyeria molecular bottom-up (de baix a dalt), aquestes nanopartícules combinen un control de mida precís amb un nombre definit de lligands a la superfície, creant una plataforma multivalent capaç d’interactuar amb els receptors cel·lulars d’una manera molt específica. En participar en el tràfic de receptors en la membrana cel·lular, obren una forma única i innovadora de modular la funció del receptor. Aquesta precisió no només permet l’eliminació efectiva de la proteïna amiloide-β del cervell, sinó que també restaura l’equilibri del sistema vascular que manté una funció cerebral saludable.
El nostre estudi va demostrar una notable eficàcia per aconseguir una ràpida eliminació d’Aβ, restaurar la funció saludable en la barrera hematoencefàlica i conduir a una sorprenent reversió de la patologia de l’Alzheimer.
Lorena Ruiz Pérez
Aquesta innovadora proposta de teràpia ofereix una via prometedora per desenvolupar intervencions clíniques efectives, abordar les contribucions vasculars a la malaltia d’Alzheimer i, en última instància, millorar els resultats dels pacients. «El nostre estudi va demostrar una notable eficàcia per aconseguir una ràpida eliminació d’Aβ, restaurar la funció saludable en la barrera hematoencefàlica i conduir a una sorprenent reversió de la patologia de l’Alzheimer», conclou Lorena Ruiz Pérez, investigadora del grup de Biònica Molecular de l’Institut de Bioenginyeria de Catalunya (IBEC) i professora adjunta Serra Hunter a la Facultat de Física de la Universitat de Barcelona (UB).
L’estudi és fruit d’una col·laboració entre l’Institut de Bioenginyeria de Catalunya (IBEC), l’Hospital West China de la Universitat de Sichuan, l’Hospital Xiamen West China de la Universitat de Sichuan, el University College de Londres, el Xiamen Key Laboratory of Psychoradiology and Neuromodulation, la Universitat de Barcelona, l’Acadèmia Xinesa de Ciències Mèdiques i la Institució Catalana de Recerca i Estudis Avançats (ICREA).
Article de referència:
Junyang Chen, Pan Xiang, Aroa Duro-Castano, Huawei Cai, Bin Guo, Xiqin Liu, Yifan Yu, Su Lui, Kui Luo, Bowen Ke, Lorena Ruiz Perez, Xiawei Wei, Qiyong Gong, Xiaohe Tian, Giuseppe Battaglia. Multivalent modulation of endothelial LRP1 induces fast neurovascular amyloid-β clearance and cognitive function improvement in Alzheimer’s disease models. Signal Transduction and Targeted Therapy (2025). DOI: 10.1038/s41392-025-02426-1





