Bacterias PAO1 infectando al pez cebra con la mutación en el promotor de nrdD (panel superior, menos verde) y con una cepa con la mutación corregida como en los aislados clínicos (panel inferior, mucho más verde).
Esta investigación, financiada parcialmente por la Fundación Española de Fibrosis Quística y por Obra Social «la Caixa», y llevada a cabo por Eduard Torrents, investigador principal en el IBEC y la estudiante de doctorado Anna Crespo, estudia nuevas estrategias para combatir las infecciones bacterianas basándose en el uso de la cepa PAO1 de la bacteria Pseudomonas aeruginosa, la cual se emplea como referencia en la mayoría de los laboratorios clínicos y de investigación.
La Pseudomonas aeruginosa es uno de los pocos microorganismos que codifica tres clases diferentes de ribonucleótido reductasa (RNR) en su genoma -una enzima esencial para la división celular de la cepa PAO1 que suministra los monómeros necesarios para la síntesis y reparación del ADN de la bacteria-, lo que le permite crecer y adaptarse a diversas condiciones ambientales, incluso durante la infección, razón por la cual se ha vuelto tan omnipresente en los laboratorios de microbiología.
Los investigadores descubrieron que la ausencia de actividad de la RNR conduce a la elongación celular en la cepa PAO1, lo que indica falta de crecimiento. Además, la expresión genética de la RNR durante la anaerobiosis –procesos que ocurren en ausencia de oxígeno- difiere entre las cepas clínicas de P. aeruginosa y las utilizadas en el laboratorio, ya que la RNR de clase III se expresa mucho más en aislados clínicos de P. aeruginosa en comparación con la cepa de laboratorio.
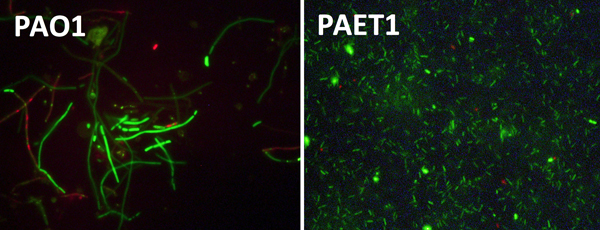
Las células bacterianas de la cepa PAO1 (izquierda) y células de un aislado clínico (derecha) crecidas en ausencia de oxígeno. La cepa PAO1 muestra claros defectos de crecimiento, con células alargadas en comparación con el aislado clínico.
«Parece que PAO1 se ha adaptado a las condiciones de laboratorio, un poco como cuando nuestros cuerpos se vuelven resistentes a los antibióticos», comenta Eduard Torrents . «Durante la infección, la P. aeruginosa clínica actúa en condiciones donde el oxígeno no está presente, pero la cepa de laboratorio PAO1 de P. aeruginosa no puede crecer de la misma manera bajo estas condiciones. En este trabajo se ha identificado que una sola mutación en la región promotora de la RNR de clase III de la cepa PAO1 interrumpe su transcripción anaeróbica, disminuyendo su virulencia. Esto significa que PAO1 no es la cepa adecuada para la investigación en condiciones anaeróbicas o de infección, ni para la búsqueda de nuevos compuestos antimicrobianos.
El descubrimiento se hizo mientras Eduard Torrents desarrollaba nuevas estrategias para combatir infecciones bacterianas y posibles dianas terapéuticas, lo que está fuertemente relacionado con la fibrosis quística. Esta enfermedad provoca la formación y acumulación de moco espeso en los pulmones, los intestinos, el páncreas y el hígado, y los pacientes sufren insuficiencia respiratoria debido a la colonización bacteriana crónica (biopelículas) en los pulmones. La investigación de Eduard Torrents está tomando un nuevo enfoque para superar este reto, desarrollando sistemas de laboratorio que imitan los pulmones de un paciente, y también introduciendo varias estrategias de nanomedicina para combatir estas infecciones.
A finales de 2016, el grupo recibió financiación de Obra Social «La Caixa», que hizo posible el triángulo de cooperación actual entre los investigadores, la clínica y la asociación de pacientes.
—
Artículo referenciado: Anna Crespo, Joan Gavaldà, Esther Julián & Eduard Torrents (2017). “A single point mutation in class III ribonucleotide reductase promoter renders Pseudomonas aeruginosa PAO1 inefficient for anaerobic growth and infection”. Scientific Reports, 7, Article number: 13350





