Les cèl·lules es mouen en grup cap a teixits rígids
El nou fenomen, anomenat durotaxi col·lectiva, obre noves vies per a controlar l’expansió tumoral i per a millorar la cicatrització de ferides.


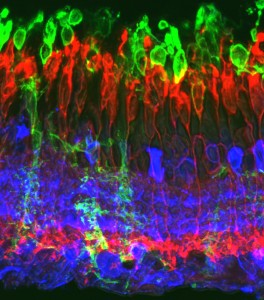
Un equip de recerca liderat per Pau Gorostiza, de l’Institut de Bioenginyeria de Catalunya (IBEC), i Amadeu Llebaria, de l’Institut de Química Avançada de Catalunya (IQAC) del CSIC, ha desenvolupat unes molècules que poden ser aplicades com a pròtesis moleculars regulades per llum per ajudar a restaurar la visió en els casos de degeneració de retina.
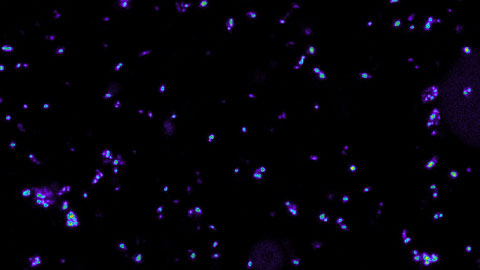 Investigadors de la UAB i de l’Institut de Bioenginyeria de Catalunya (IBEC) han descobert una manera efectiva d’administrar el micobacteri M. brumae necessàri pel tractament de càncer de bufeta en humans
Investigadors de la UAB i de l’Institut de Bioenginyeria de Catalunya (IBEC) han descobert una manera efectiva d’administrar el micobacteri M. brumae necessàri pel tractament de càncer de bufeta en humansEls investigadors han trobat una forma de reduir la formació dels grumolls naturals que es produeixen quan s’introdueix els micobacteris, que posseeixen un alt contingut de lípids en les seves parets, en les solucions aquoses que habitualment s’utilitzen per a la instil·lació intravesical – l’aplicació directa de medicament mitjançant degoteig -en pacients amb càncer de bufeta.
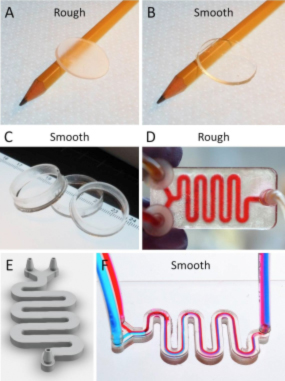 Amb la impressió 3D es revolucionarà la recerca, els investigadors de l’IBEC han estat explorant les possibilitats que ofereix la nova tecnologia per millorar els seus processos i mètodes.
Amb la impressió 3D es revolucionarà la recerca, els investigadors de l’IBEC han estat explorant les possibilitats que ofereix la nova tecnologia per millorar els seus processos i mètodes.Recentment l’IBEC s’ha convertit en la llar de la primera bioimpressora 3D de Catalunya, que promet obrir noves vies en el camp de regeneració de teixits i òrgans. No obstant això, en una col·laboració amb la UPF, el CINVESTAV-Monterrey, a Mèxic, i la Universitat de Washington, els científics amb seu a Barcelona, van desenvolupar una nova forma de produir dispositius microfluídics – sistemes en què obtenen baixos volums de fluids.
L’estudi, publicat en la revista Light: Science & Applications, del grup editorial Nature, revela per primera vegada, que la il·luminació amb longituds d’ona més llargues implica una menor dispersió dels fotons que viatgen a través dels teixits.
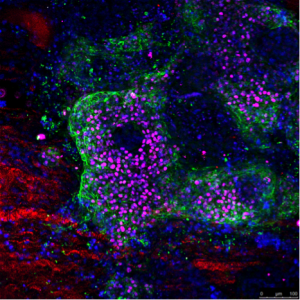 Investigadors de l’Institut de Bioenginyeria de Catalunya (IBEC), en col·laboració amb l’Hospital General Universitari Gregorio Marañón i dos grups dels EUA han creat, per primera vegada, empelts de cor a partir de cèl·lules mare pluripotents humanes en un període inferior a un mes.
Investigadors de l’Institut de Bioenginyeria de Catalunya (IBEC), en col·laboració amb l’Hospital General Universitari Gregorio Marañón i dos grups dels EUA han creat, per primera vegada, empelts de cor a partir de cèl·lules mare pluripotents humanes en un període inferior a un mes.L’estudi, publicat recentment en la revista Biomaterials, descriu com els investigadors han descel·lularitzat cors humans qualificats com “no aptes per al trasplantament” per l’Organització Nacional de Trasplantaments, deixant la matriu extracel·lular intacta i lliure de cèl·lules, i a continuació, l’han repoblat amb cèl·lules cardíaques obtingudes a partir de tècniques d’edició del genoma en cèl·lules mares pluripotents humanes (hPSCs) (cèl·lules no diferenciades, a partir de les quals es poden desenvolupar altres tipus cel·lulars). Les cèl·lules mare pluripotents són crucials per a aquest procés, ja que el cos no és capaç de generar noves cèl·lules cardíaques després d’un atac al cor o un altre tipus de dany cardíac.
 Investigadors de la unitat mixta de Nanomalaria IBEC/ISGlobal, han trobat molècules similars a l’heparina, aïllades a partir de cogombres de mar, algues vermelles i esponges marines, que inhibeixen el creixement del Plasmodium falciparum, un dels paràsits causants de la malària. A diferència de l’heparina, aquestes molècules tenen una activitat reduïda com a anticoagulant sanguini, la qual cosa obre noves vies per al desenvolupament de medicaments antimalàrics.
Investigadors de la unitat mixta de Nanomalaria IBEC/ISGlobal, han trobat molècules similars a l’heparina, aïllades a partir de cogombres de mar, algues vermelles i esponges marines, que inhibeixen el creixement del Plasmodium falciparum, un dels paràsits causants de la malària. A diferència de l’heparina, aquestes molècules tenen una activitat reduïda com a anticoagulant sanguini, la qual cosa obre noves vies per al desenvolupament de medicaments antimalàrics.Quan el paràsit de la malària entra en el torrent sanguini, envaeix les cèl·lules del fetge per produir milers de merozoïts (una fase del cicle de vida del paràsit Plasmodium). Aquests merozoïts tornen a incorporar-se al torrent, on infecten els glòbuls vermells i aconsegueixen escapar a la vigilància del sistema immunitari.
 Investigadors de la Universitat de Barcelona (UB) i de l’Institut de Bioenginyeria de Catalunya (IBEC) juntament amb els seus col·laboradors han definit un nou tipus de marcadors de virulència bacteriana que poden ajudar a detectar i prevenir els brots d’infeccions provocats per Escherichia coli.
Investigadors de la Universitat de Barcelona (UB) i de l’Institut de Bioenginyeria de Catalunya (IBEC) juntament amb els seus col·laboradors han definit un nou tipus de marcadors de virulència bacteriana que poden ajudar a detectar i prevenir els brots d’infeccions provocats per Escherichia coli. La majoria de les soques bacterianes d’ E. coli, es troben de forma natural en l’intestí humà i no suposen cap risc per a la salut, a excepció de determinats tipus d’aquests bacteris (patotip), alguns dels quals causen intoxicacions alimentàries que pot arribar a ser mortals. Una d’aquestes soques virulentes d’E. coli, el serotip O104: H4, va causar un important brot infecciós a Alemanya durant l’any 2011, associat a una alta prevalença de la síndrome hemolític-urèmic. Es tractava d’una soca d’evolució recent que va fer que es registrés l’índex més gran de mortaldat per E. coli de tots els temps.
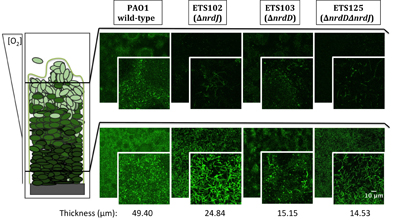 Investigadors de l’Institut de Bioenginyeria de Catalunya (IBEC) estan més a prop de comprendre com els bacteris provoquen infeccions cròniques mitjançant la identificació dels enzims clau que els permeten crear les condicions adequades per a la infecció en forma de biopel·lícula, la qual cosa ajudarà a millorar el disseny de fàrmacs antibacterians específics.
Investigadors de l’Institut de Bioenginyeria de Catalunya (IBEC) estan més a prop de comprendre com els bacteris provoquen infeccions cròniques mitjançant la identificació dels enzims clau que els permeten crear les condicions adequades per a la infecció en forma de biopel·lícula, la qual cosa ajudarà a millorar el disseny de fàrmacs antibacterians específics.Quan els bacteris P. aeruginosa provoquen infeccions cròniques de pulmó, com per exemple en pacients de Fibrosi Quística o de Malaltia Pulmonar Obstructiva Crònica (EPOC), significa que han estat capaces de formar una biopel·lícula madura in situ que els permet créixer i adaptar-se.
 Investigadors de l’Institut de Bioenginyeria de Catalunya (IBEC) han descobert el mecanisme mitjançant el qual la rigidesa del teixit activa el càncer. Aquest nou coneixement obre portes cap a nous tractaments per frenar, o fins i tot detenir, el creixement de tumors.
Investigadors de l’Institut de Bioenginyeria de Catalunya (IBEC) han descobert el mecanisme mitjançant el qual la rigidesa del teixit activa el càncer. Aquest nou coneixement obre portes cap a nous tractaments per frenar, o fins i tot detenir, el creixement de tumors.Els resultats, fruit de la col·laboració entre investigadors de l’IBEC i de l’Institute of Technology de Geòrgia, es publiquen avui a la prestigiosa revista Nature Cell Biology, on s’identifica el mecanisme mitjançant el qual la rigidesa del teixit activa un important oncogen anomenat YAP.