Después de una lesión aguda, como un infarto de miocardio, el corazón humano es incapaz de regenerarse. Las células cardíacas adultas no pueden crecer y dividirse para sustituir a las dañadas, y la lesión se vuelve irreversible. Pero esto no pasa en todos los animales. Un pez de agua dulce originario del Sudeste Asiático, conocido como pez cebra, puede regenerar su corazón por completo incluso después de la amputación del 20% de su ventrículo.
Esta capacidad regenerativa extraordinaria ha llamado la atención de investigadores de todo el mundo, que ven el abanico de posibilidades que se abriría si este mecanismo de regeneración se pudiera aplicar en terapias para humanos.
En un artículo publicado hoy a la revista Nature Materials, un equipo de investigadores del Instituto de Bioingeniería de Cataluña (IBEC) dirigido por Xavier Trepat, en colaboración con el Centro de Medicina Regenerativa de Barcelona (CMR[B]), han descubierto un sorprendente mecanismo por el cual las células cardíacas del pez cebra se mueven y dividen durante la regeneración.

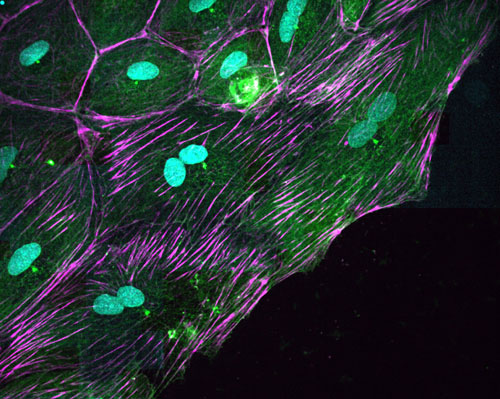
Los investigadores se han centrado en el epicardio, que es la capa de células que recubre el corazón. A pesar de que las células del epicardio representan solo una pequeña fracción de la masa del corazón, juegan un papel fundamental en su regeneración. “El epicardio es el origen de varios tipos celulares del corazón, y secreta señales bioquímicas que indican al resto de células qué tienen que hacer en cada momento. Es un tipo de ‘hub’ de la regeneración”, indica Angel Raya, Investigador ICREA y director del CMRB.
Después de una lesión, las células del epicardo empiezan a dividirse y moverse en masa para recubrir la herida. Los investigadores han observado que durante este proceso las células se vuelven bi-nucleadas: duplican el material genético y lo separan en dos núcleos, pero no se llegan a dividir en dos células independientes. “Nos sorprendió mucho descubrir células que en vez de tener un núcleo, como es habitual en la mayoría de tejidos, tienen dos, y cada uno de ellos contiene una copia del ADN de la célula” afirma Trepat, investigador ICREA en el IBEC y profesor asociado de la Universitat de Barcelona.
Los investigadores han descubierto que el mecanismo por el cual las células se vuelven bi-nucleadas es de origen biomecánico. Una vez el ADN ya se ha separado en dos núcleos, la mayoría de células animales forman un anillo contráctil en su ecuador. A medida que se va contrayendo, esta anillo divide la célula madre en dos células hijas. En el caso de las células del corazón del pez cebra, el estudio muestra que el anillo se adhiere a las fibras de su entorno de manera que no se puede contraer. El resultado es que las dos células hijas no pueden llegar a separarse a pesar de haber duplicado correctamente su ADN.
“La multinucleación es un fenómeno muy conocido en cáncer, porque es una causa de inestabilidad genómica. Es decir, las células cancerosas pierden el control de las proteínas que sintetizan y se comportan patológicamente. En el caso del corazón de pez cebra, la multinucleación es fisiológica y no parece causar ningún problema”, afirma Marina Uroz, primer autora del artículo. El siguiente paso será estudiar qué papel tienen las células multinucleadas durante la regeneración del corazón y otros órganos.
El Dr. Trepat y el Dr. Raya forman parte del CIBER-BBN (Centro de Investigación Biomédica en Red en Bioingeniería, Biomateriales y Nanomedicina).
Artículo de referencia: M. Uroz, A. Garcia-Puig, I. Tekeli, A. Elosegui-Artola, J. F. Abenza, A. Marín-Llauradó, S. Pujals, V. Conte, L. Albertazzi, P. Roca-Cusachs, A. Raya and X. Trepat. Traction forces at the cytokinetic ring regulate cell division and polyploidy in the migrating zebrafish epicardium. Nature Materials, DOI: 10.1038/s41563-019-0381-9 (2019)





